
2022年,军事医学研究院裴雪涛/李艳华团队联合天津大学医学部张健课题组在干细胞领域期刊Cell Stem Cell在线发表了题为:Direct chemical reprogramming of human cord blood erythroblasts to induced megakaryocytes that produce platelets的研究文章。运用化学重编程技术实现了人成红细胞向巨核细胞及血小板的命运转换,并利用单细胞转录组和染色质开放性测序技术系统追踪了该过程中的细胞动态变化。安诺优达为本次研究提供了10x单细胞转录组测序服务。

研究背景
血小板(blood platelet,PLT)是血液有形成分之一,是成熟巨核细胞裂解脱落下来的具有生物活性的无核细胞。血小板输注是临床治疗血小板减少症、防治出血和挽救生命的主要手段之一。临床上,血小板供应主要靠健康献血者捐赠。但是,血小板存储时间短且易被污染。因此,亟需运用新技术解决血小板来源问题。对此,基于干细胞技术、细胞重编程技术获取巨核细胞及血小板的研究一直是国际竞争的前沿与热点领域之一。
在细胞重编程的研究中,种子细胞的选择对于能否成功而有效地启动细胞命运转换至关重要。成红细胞是存在于骨髓、外周血和脐带血中的一种有核红细胞,成红细胞和巨核细胞在发育过程中来自共同的前体,即巨核-红系共祖细胞,它们之间紧密的谱系联系使得成红细胞成为获得巨核细胞理想的候选种子细胞。
材料选择
初始成红细胞(D0)和第3天(D3)、第5天(D5)以及第7天(D7)的重编程细胞
研究思路
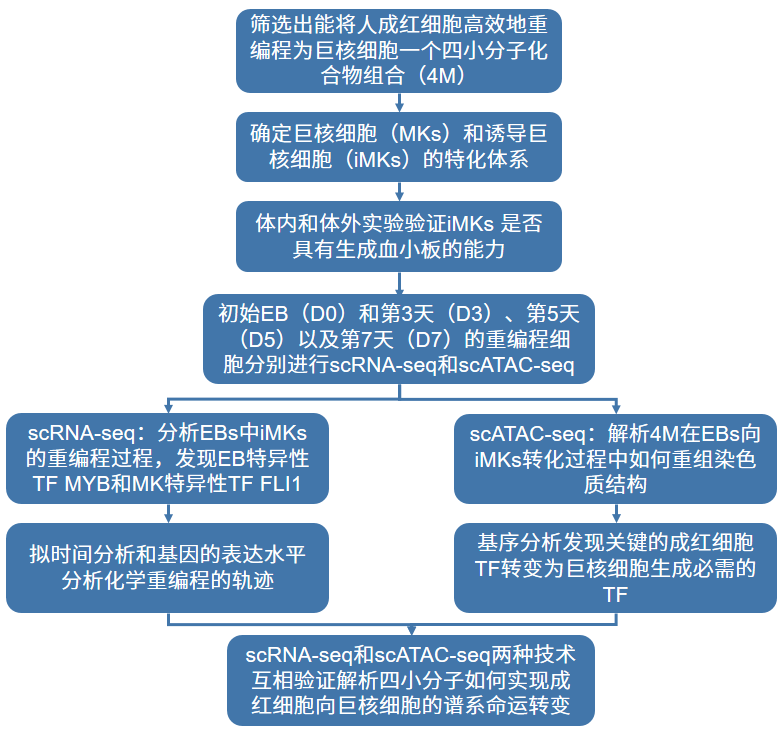
研究结果
4M“cocktail”可以激活EBs的MK命运
通过流式细胞术扩增并纯化获得脐带血(CB)成红细胞(EB)。作者选择4个小分子(4M;Bix01294、RG108、VPA和PD0325901)作为筛选cocktail的基线。通过流式细胞术分析两种巨核细胞(MK)特异性细胞表面标记物CD41a和CD42b的表达,定义了在4M“cocktail”条件下存在持续7天的MK诱导期。通过观察GFP+细胞感染慢病毒PF4-GFP,作者发现4M“cocktail”在5和7天重编程阶段逐渐启动了由PF4启动子驱动的GFP表达(图1G和1H)。
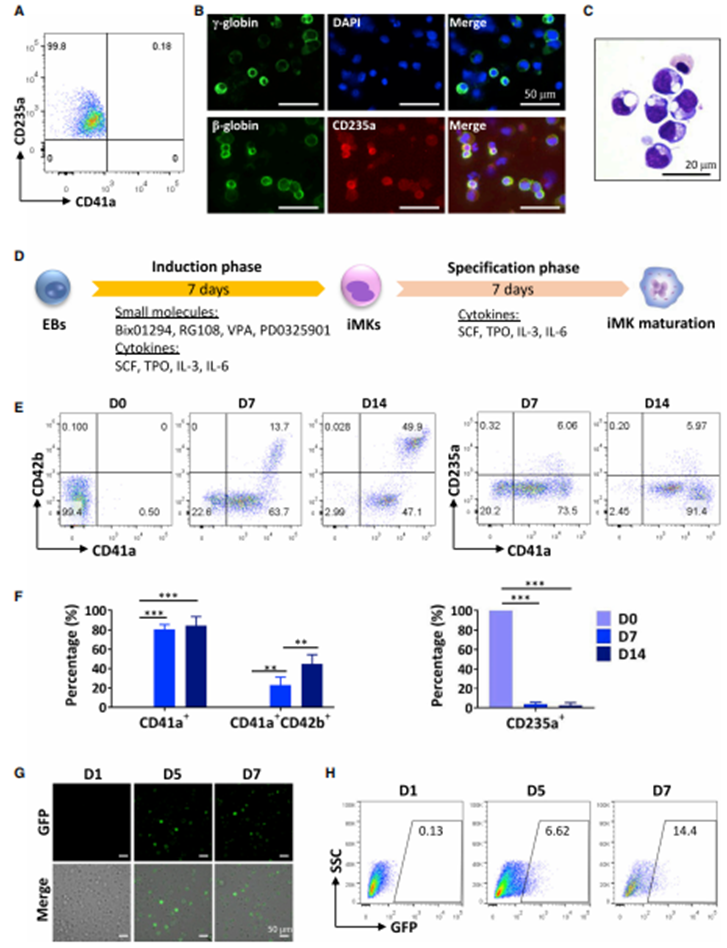
图1 小分子诱导EB重编程为iMKs
两相诱导后的EB衍生的iMKs具有MK特性
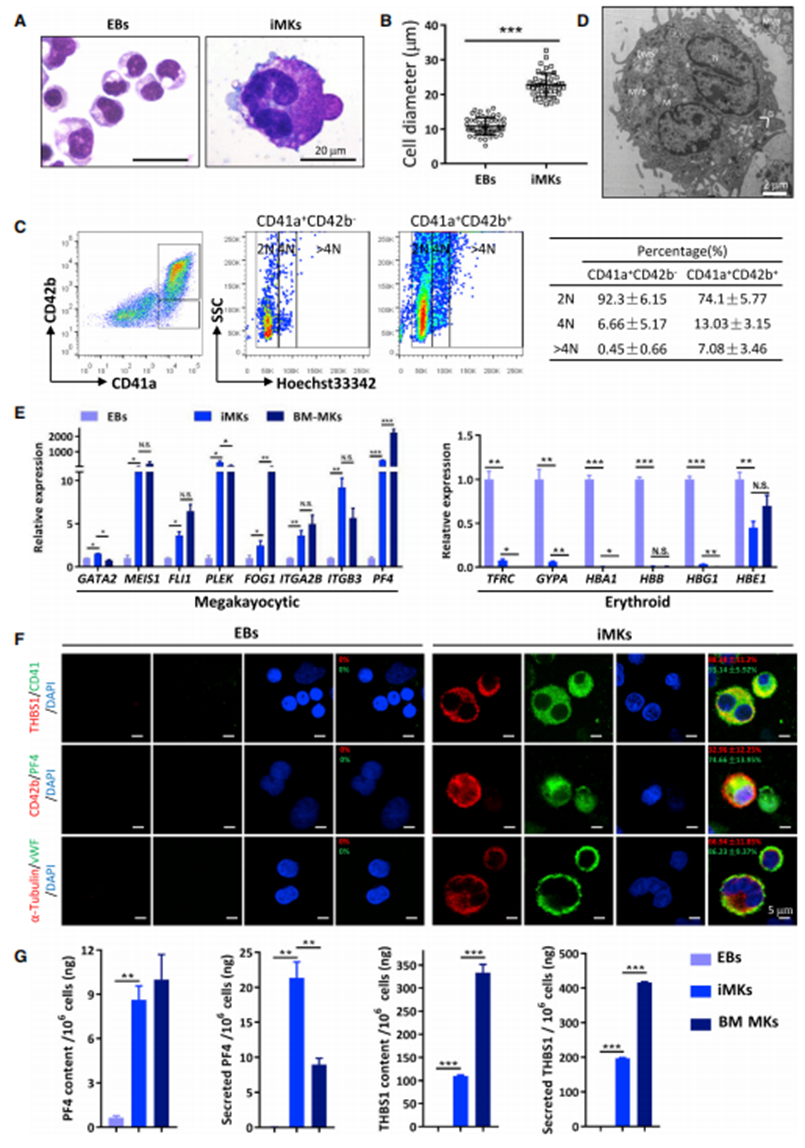
图2 iMKs的特性
EB诱导的iMKs可在体外产生前血小板和功能性血小板
为了探究iMKs是否能在体外产生前血小板和PLT,作者将第14天的iMKs转移到MK成熟培养基中,培养7天后,发现这些分化的促血小板样细胞表达CD41、CD42b和vWF(图3B),表明iMKs成熟为促血小板。通过流式细胞仪分析,作者检测到这些前血小板能够产生PLT。免疫荧光染色显示,iMK-PLTs表达高水平的PLT特征蛋白。
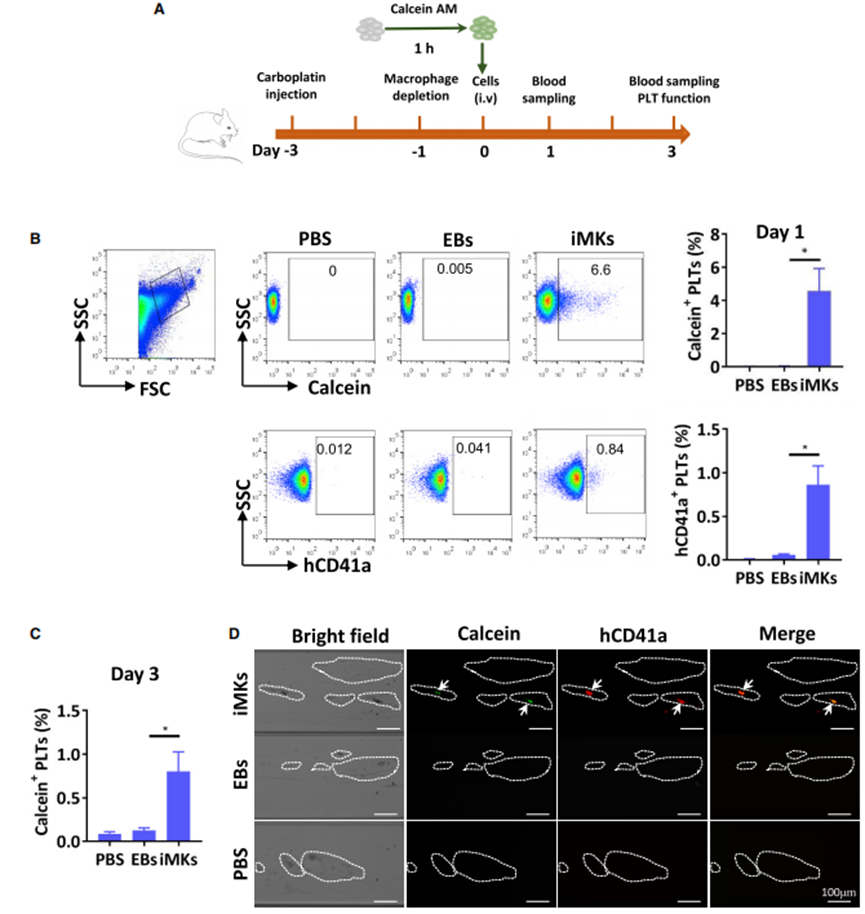
图3 iMK-PLTs的体外表征
iMKs可以在体内产生功能性血小板
为了评估iMKs是否能在体内产生功能性PLTs,作者采用血小板减低症的免疫缺陷小鼠进行实验验证,发现来自EB的iMKs将人PLT释放到小鼠血液循环中,iMKs可以在体内持续产生人PLT。作者又在细胞输血后第3天从血小板减低症的免疫缺陷小鼠中收集了PLT-rich血浆(PRP)。通过自动微流控室系统评估血栓形成,发现在所有PRP样品中均有血栓生成(图4D)。
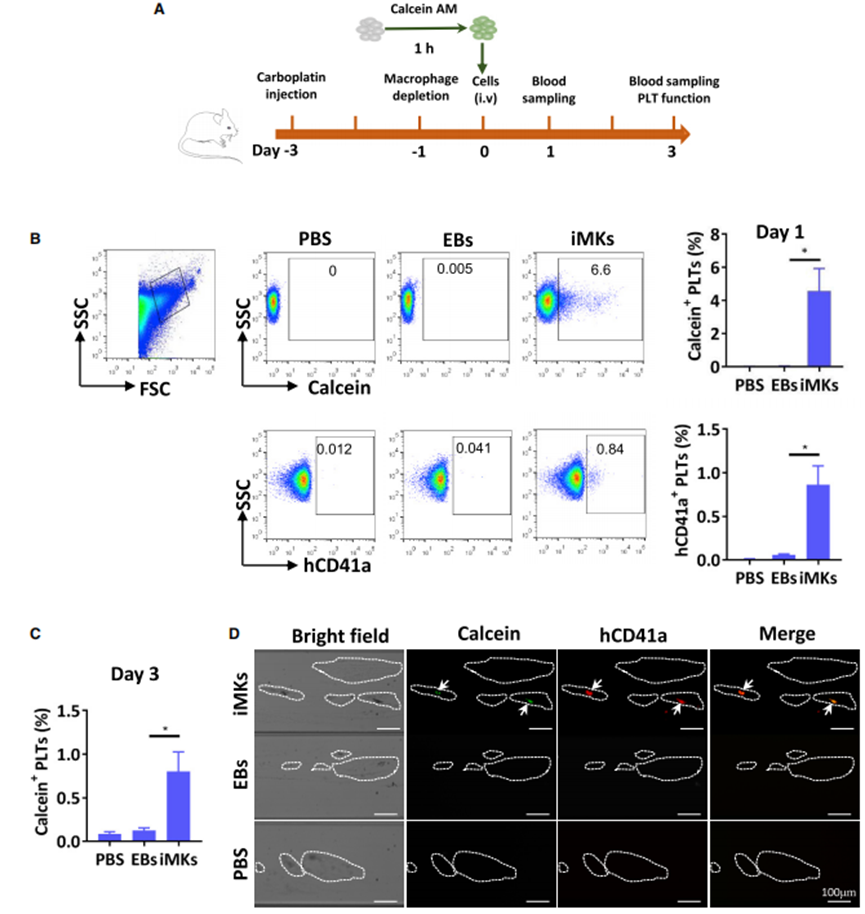
图4 诱导巨核细胞(iMKs)在体内产生功能性PLT
scRNA-seq分析确定了MK命运获取的进程,并描述了重编程路径
为了分析EBs中iMKs的重编程过程,作者使用10x Genomics平台对EBs第0天(D0)和重编程第3天(D3)、第5天(D5)和第7天(D7)的细胞进行了单细胞基因表达谱分析,共捕获了24967个细胞,鉴定出6个转录不同的聚类。C1期和C2期的大部分细胞处于G2M期或S期,表明这些细胞处于活性增殖状态。C3是C1、C2、C4和C5之间的中间状态。C4和C5其关键巨核细胞基因RGS18、F2R、PPBP、PF4的表达水平相似,定义为iMK-1和iMK-2(图5C和5D)。其中iMK-1为血小板生成偏向性强的巨核细胞;iMK-2是免疫偏向性的巨核系细胞,可能在免疫调节、炎症调节过程中发挥作用。作者选择CD53来区分这两个群体,发现重编程系统更有利于iMK-1的生成。
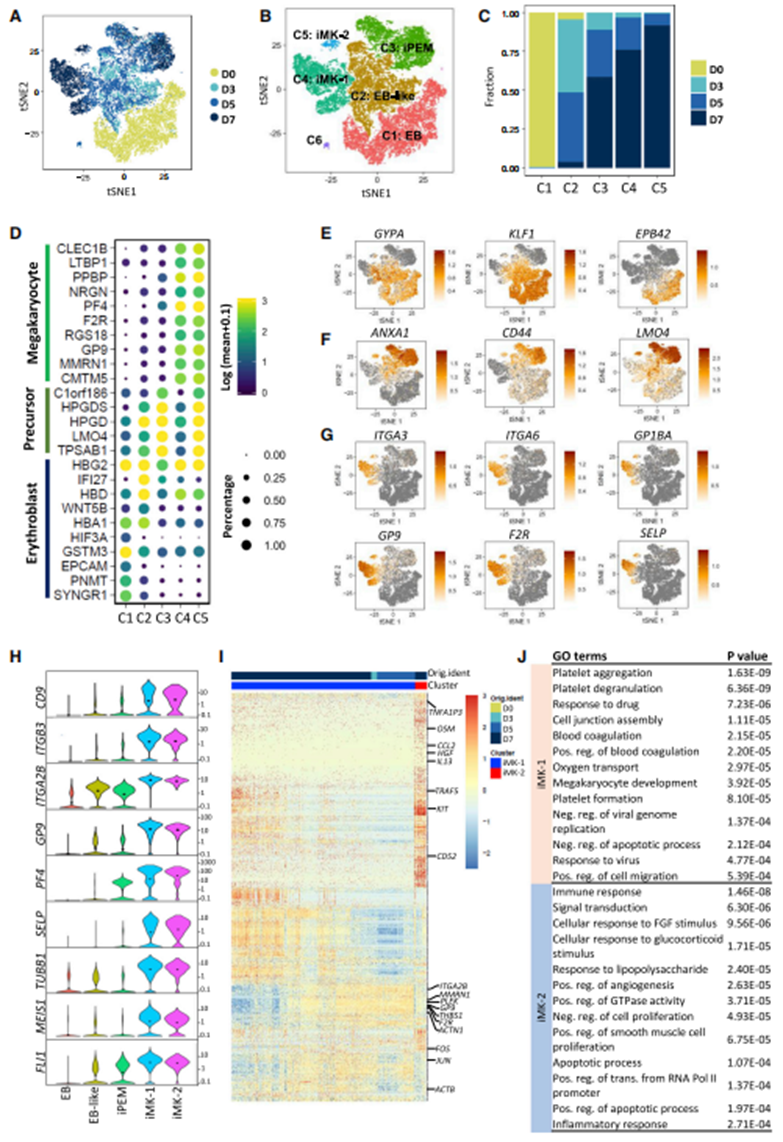
图5 使用scRNA-seq对从EBs到iMKs的4M重编程进行高分辨率解析
4M“cocktail”通过染色质重塑诱导EB向iMK的重编程
为了了解4M在EBs向iMKs转化过程中如何重组染色质结构,ATAC-seq分析发现,在4M诱导后,在重编程细胞中,红系主调控因子具有封闭的染色质状态,染色质水平的重编程和这些TFs协调EB细胞和MK细胞的命运转变。重编程过程中关键转录因子的染色质状态,红细胞发育的主TF基因,MYB和KLF1的表达随着重编程路径逐渐减少,与scRNA-seq数据结果显示一致。总之,4M的重编程机制可能涉及降低红细胞必需TF基因的染色质可及性,并开放EB和MK关键TF基因的调控区域,从而驱动MK命运的规范。
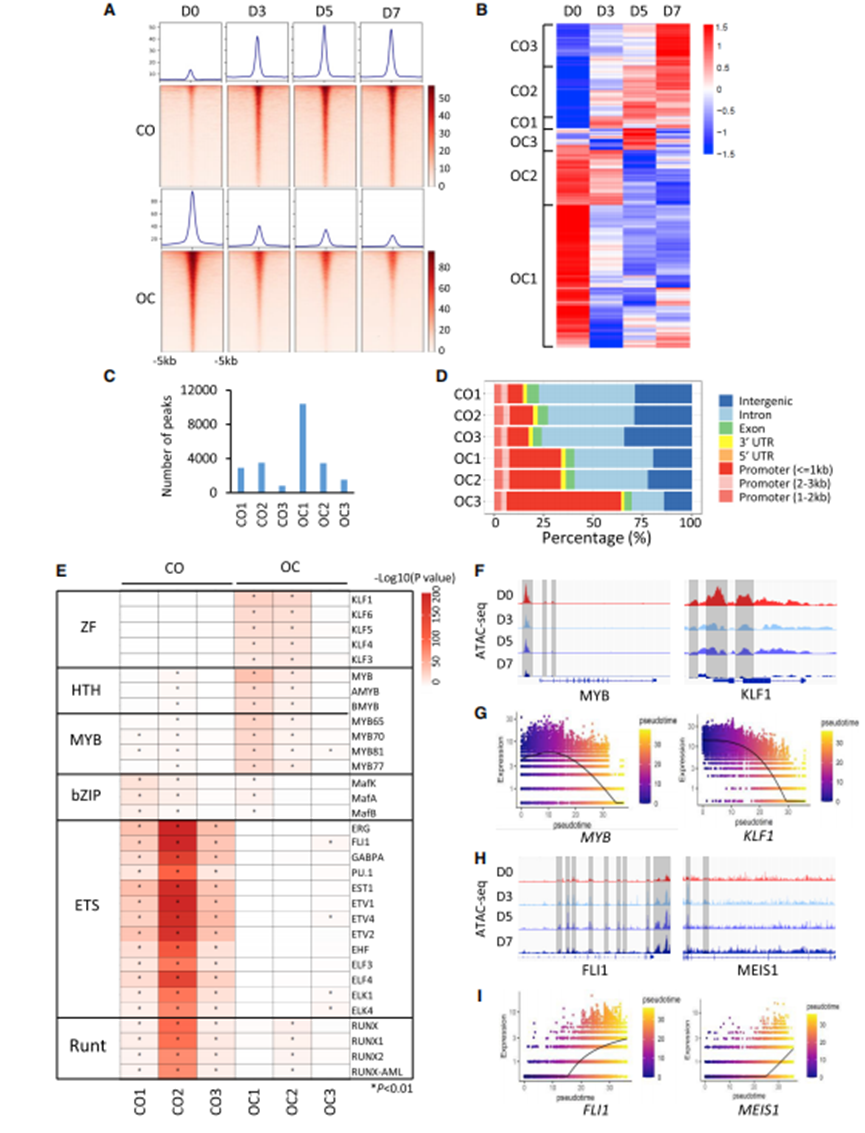
图6 ATAC-seq揭示重编程过程中的染色质动力学
结论
本研究独辟蹊径,仅运用小分子化合物成功实现成红细胞向功能性巨核细胞及血小板的命运转变,为体外大规模人工制备巨核细胞和血小板开辟了新的路径。
参考文献
Qin J, Zhang J, Jiang J, Zhang B, Li J, Lin X, Wang S, Zhu M, Fan Z, Lv Y, He L, Chen L, Yue W, Li Y, Pei X. Direct chemical reprogramming of human cord blood erythroblasts to induced megakaryocytes that produce platelets[J]. Cell Stem Cell. 2022 Aug 4;29(8):1229-1245.e7. doi: 10.1016/j.stem.2022.07.004.